Предистория и дизайн на изследването
Ретатрутид (LY3437943) е ново лекарство с един пептид, което активиратри рецептора едновременно: GIP, GLP-1 и глюкагон. За да се оцени ефикасността и безопасността му при лица със затлъстяване, но без диабет, беше проведено рандомизирано, двойносляпо, плацебо-контролирано проучване фаза 2 (NCT04881760). Общо338 участницис ИТМ ≥30 или ≥27 с поне едно съпътстващо заболяване, свързано с теглото, бяха рандомизирани да получават плацебо или ретатрутид (1 mg, 4 mg с две схеми на титриране, 8 mg с две схеми на титриране или 12 mg), прилаган веднъж седмично чрез подкожна инжекция в продължение на 48 седмици.първична крайна точкабеше процентната промяна в телесното тегло на 24-та седмица, с вторични крайни точки, включващи промяна в теглото на 48-та седмица и категорични прагове за загуба на тегло (≥5%, ≥10%, ≥15%).
Ключови резултати
-
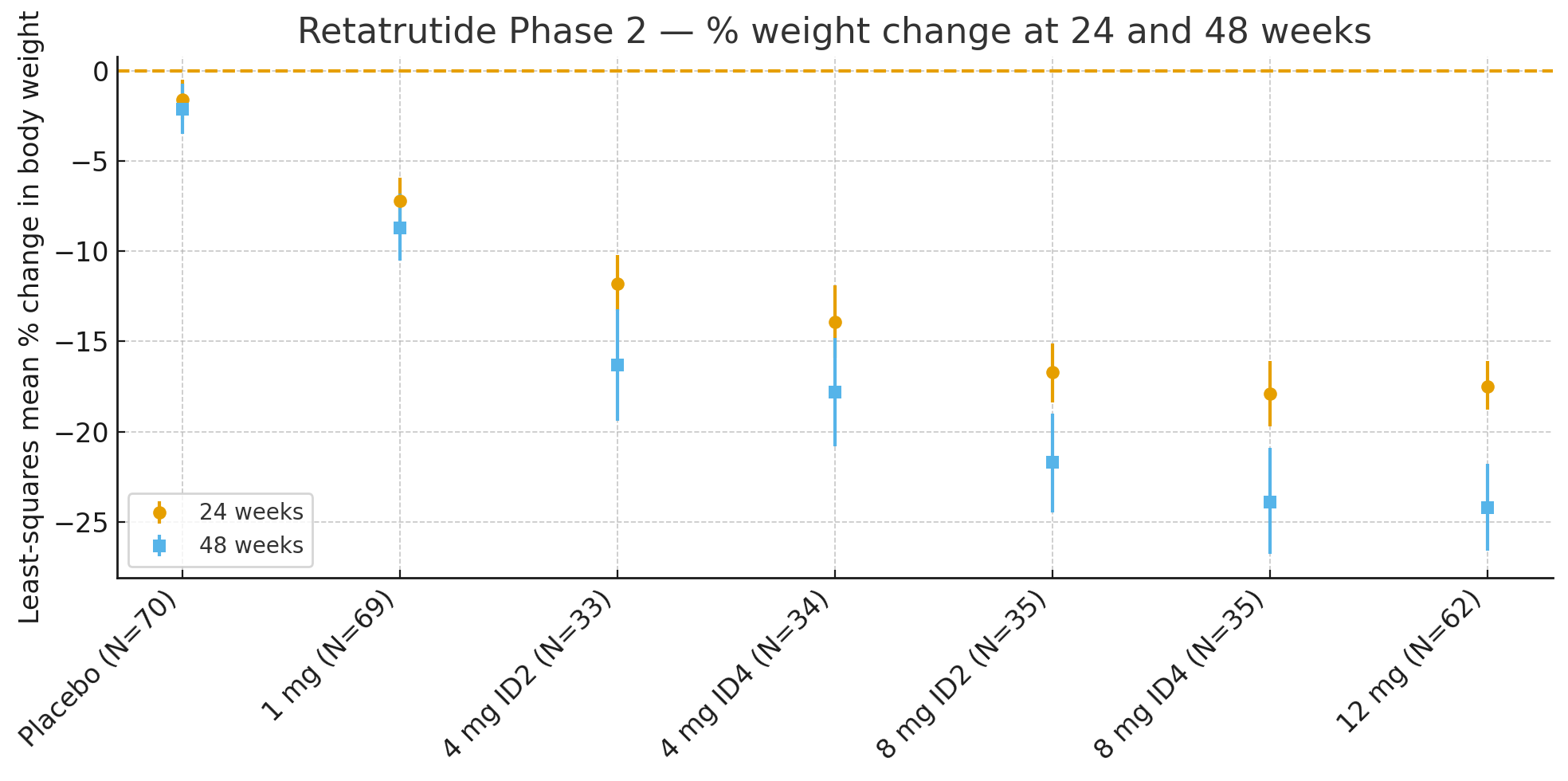
24 седмициСредната процентна промяна в телесното тегло спрямо изходното ниво, измерена по метода на най-малките квадрати, беше
-
Плацебо: −1,6%
-
1 мг: −7,2%
-
4 мг (комбинирано): −12,9%
-
8 мг (комбинирано): −17,3%
-
12 мг: −17,5%
-
-
48 седмициПроцентната промяна в телесното тегло беше
-
Плацебо: −2,1%
-
1 мг: −8,7%
-
4 мг (комбинирано): −17,1%
-
8 мг (комбинирано): −22,8%
-
12 мг: −24,2%
-
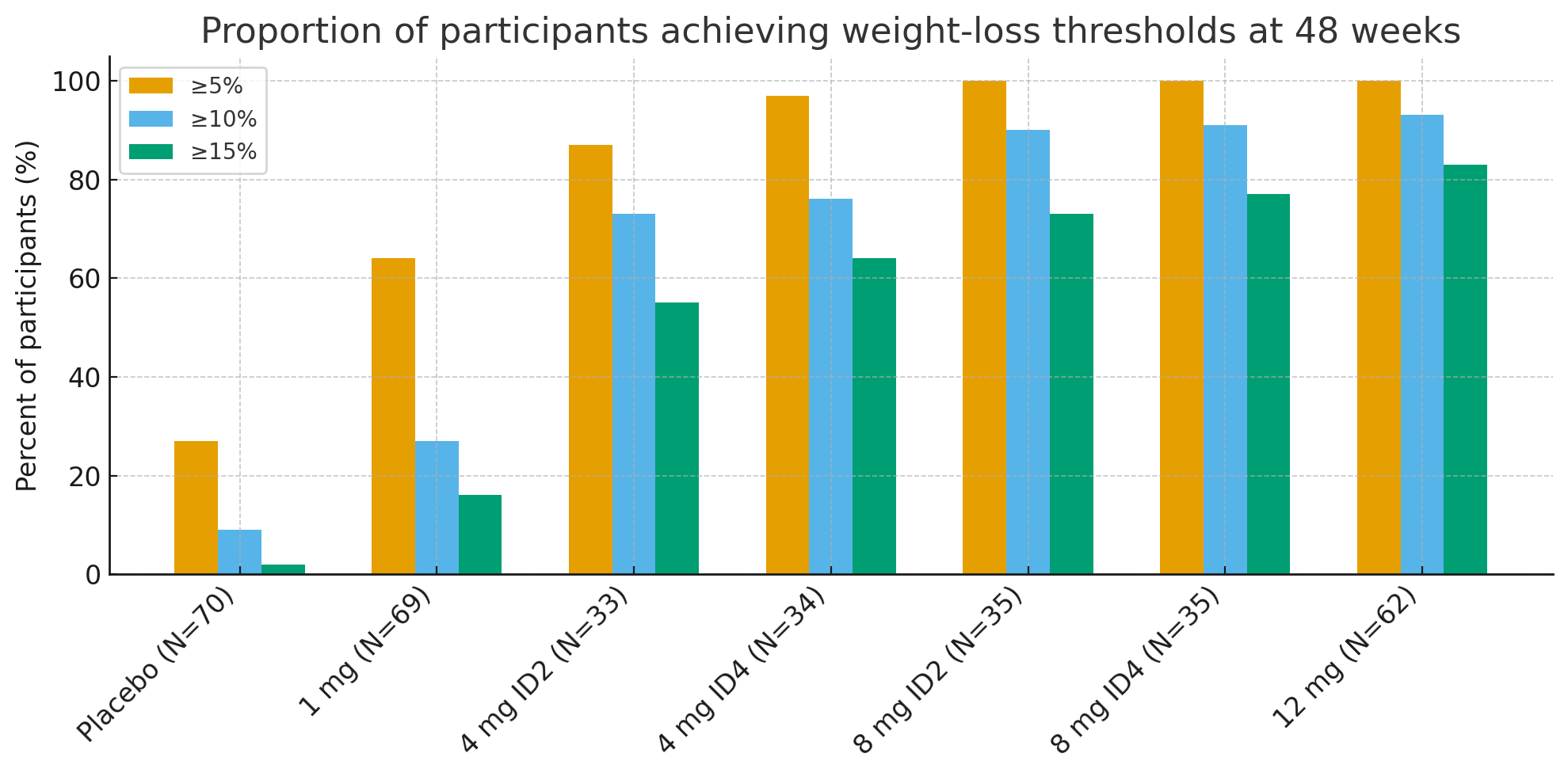
На 48-та седмица, процентът на участниците, постигнали клинично значими прагове за загуба на тегло, бил поразителен:
-
≥5% загуба на тегло: 27% с плацебо спрямо 92–100% в активните групи
-
≥10%: 9% с плацебо спрямо 73–93% в активните групи
-
≥15%: 2% с плацебо спрямо 55–83% в активните групи
В групата с 12 mg, до26% от участниците са загубили ≥30% от изходното си тегло, степен на загуба на тегло, сравнима с бариатричната хирургия.
Безопасност
Най-честите нежелани реакции са били стомашно-чревни (гадене, повръщане, диария), обикновено леки до умерени и дозозависими. По-ниските начални дози (титриране на 2 mg) са намалили тези реакции. Наблюдавано е дозозависимо повишаване на сърдечната честота, достигащо пик на 24-та седмица, след което намалява. Честотата на прекъсване на лечението варира от 6 до 16% в активните групи, малко по-висока от тази при плацебо.
Заключения
При възрастни със затлъстяване без диабет, седмичното подкожно приложение на ретатрутид в продължение на 48 седмици е довело дозначително, дозозависимо намаляване на телесното тегло(до ~24% средна загуба при най-високата доза), заедно с подобрения в кардиометаболните маркери. Стомашно-чревните нежелани реакции бяха чести, но овладяеми с титриране. Тези открития от фаза 2 показват, че ретатрутид може да представлява нов терапевтичен бенчмарк за затлъстяване, в очакване на потвърждение в по-големи, дългосрочни проучвания от фаза 3.
Време на публикуване: 28 септември 2025 г.